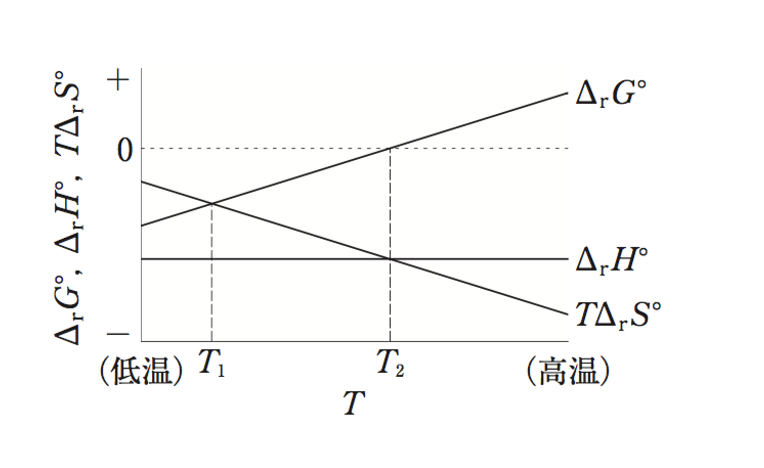
生体における化学反応は約37 ℃で進行するが、化学反応は温度の影響をうけるため熱力学パラメーターの温度依存性を知ることは重要なことである。圧力一定条件下での温度Tと熱力学パラメータ(ΔrG°、ΔH°、TΔrS°)の関係が図のようになる化学反応に関する記述のうち、正しいのはどれか。2つ選べ。ただし、ΔrG°、ΔH°、TΔrS°は、それぞれ標準反応ギブズエネルギー、標準反応エンタルピー、標準反応エントロピーを表す。
- この化学反応は、発熱反応である。
- 温度T1での平衡定数は、温度T2での平衡定数よりも小さい。
- 温度がT2より高温側での平衡定数は、1より小さい。
- 温度がT2より低温側では、この反応はエントロピー駆動となる。
- 温度がT2よりも低温側では、反応の進む向きは反応物と生成物の初期濃度に依存しない。





コメント