解答
7
動画解説
解説
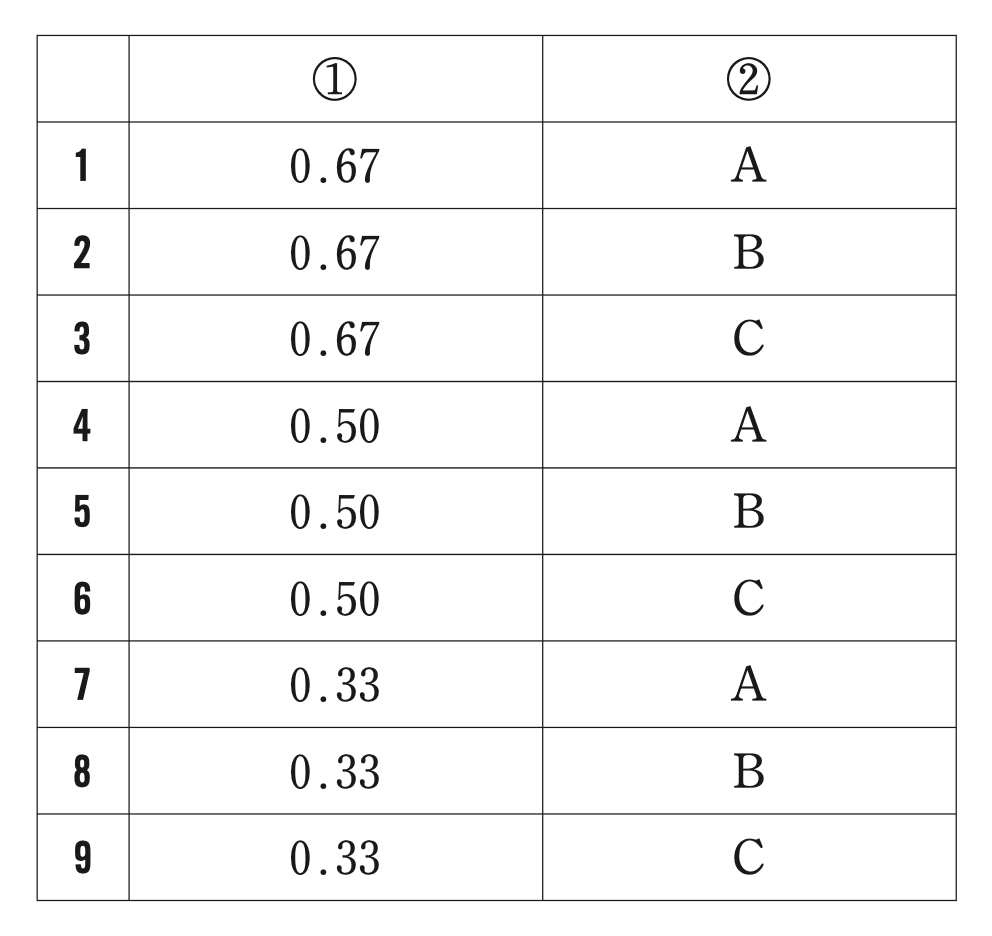
①
<理想溶液の蒸気圧を求める>
ラウールの法則より理想溶液の蒸気圧を以下のように求めることができる。
純Xの蒸気圧が500 hPaであり、そのモル分率が0.5であることから、Xが示す蒸気分圧=500 hPa×0.5=250 hPaとなり、また、純Yの蒸気圧が1000 hPaであり、そのモル分率が0.5であることから、Yが示す蒸気分圧=1000 hPa×0.5=500 hPaとなる。
これらのことより、理想溶液の蒸気圧=250 hPa+500 hPa=750 hPaとなる。
<蒸気における各成分のモル分率を求める>
設問に「平衡にある」となっていることから、溶液における蒸気圧と蒸気における蒸気圧が等しいと考えられる。よって、ドルトン分圧の法則より、蒸気分圧から、各成分のモル分率を以下のように求めることができる。
Xのモル分率=250 hPa/750 hPa=0.33
Yのモル分率=500 hPa/750 hPa=0.67
②
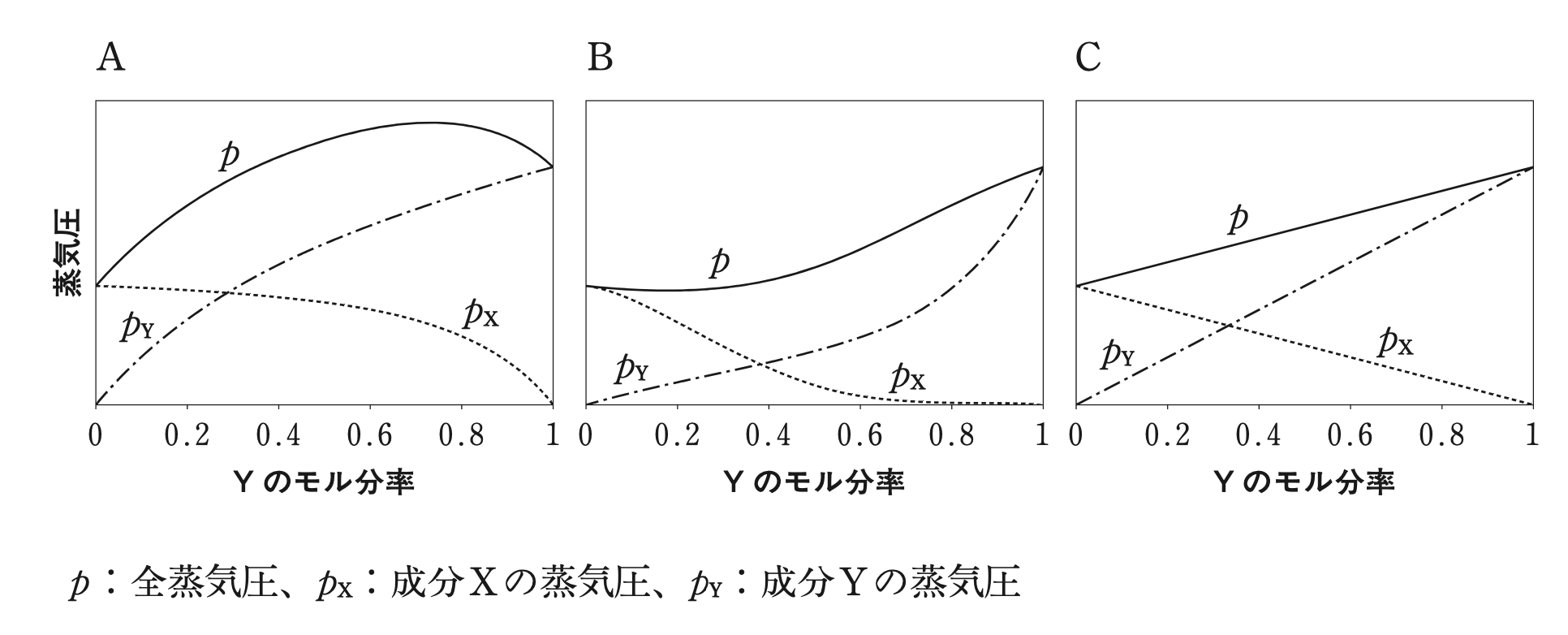
設問に「成分X、Yが理想溶液とみなせず、XとYの分子間相互作用が同種分子間の相互作用よりも弱い場合」とあることから、XとYを混合すると活量係数が1より大きくなり、Aのようなグラフになる。
参考
・ラウールの法則
理想溶液の蒸気圧=純物質の蒸気圧×モル分率
・ドルトン分圧の法則
理想気体の蒸気圧=全蒸気圧×モル分率





コメント
コメント一覧 (1件)
[…] 第100回 問93 […]