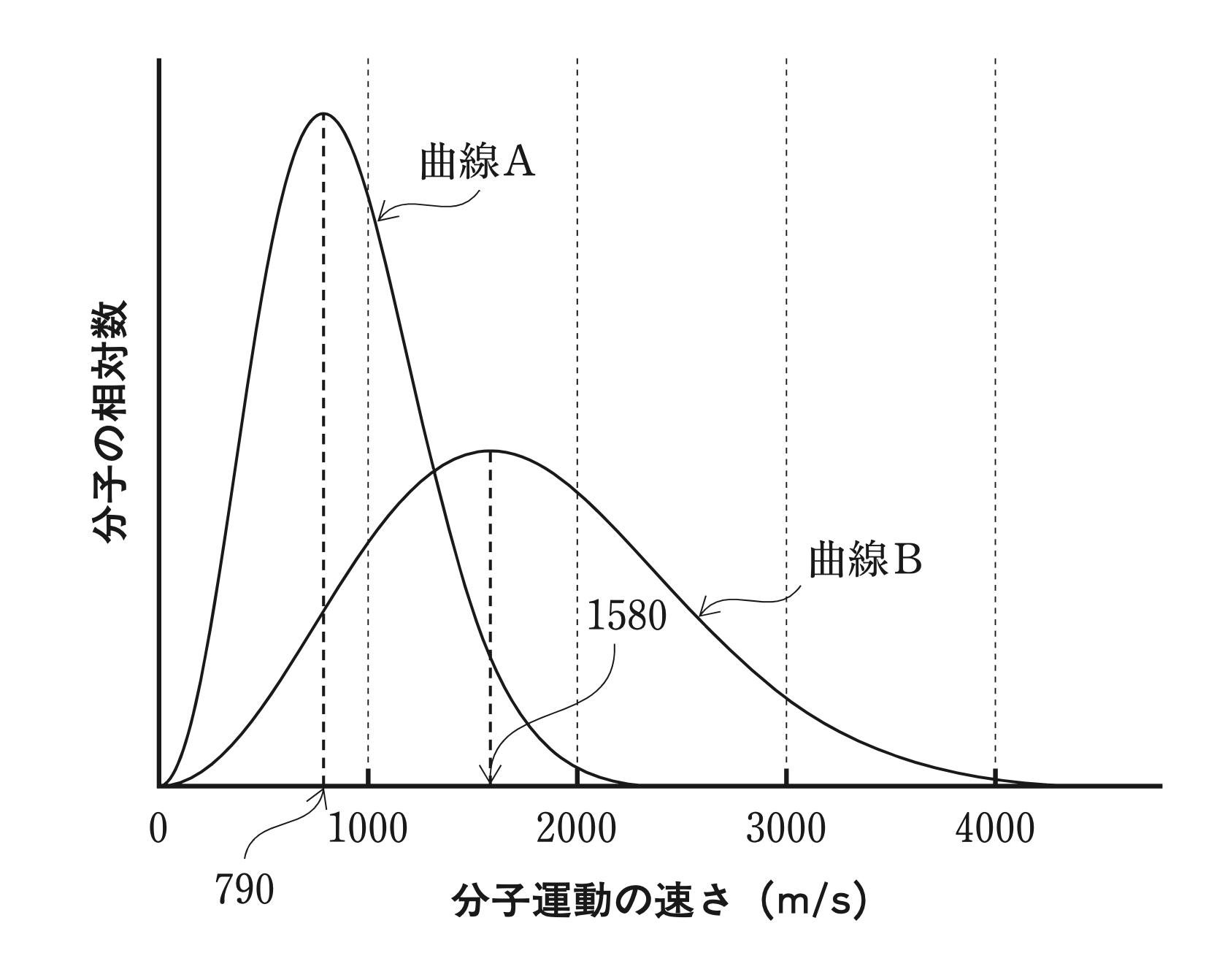
下の図は、マクスウェル・ボルツマン分布則に基づいた、温度の異なる、ある理想気体の運動の速さ分布である。図中の曲線Aは温度T1=150 Kの場合、曲線Bは温度T2の場合を示す。気体の運動に関する記述のうち、正しいのはどれか。2つ選べ。ただし、図中の分子運動は並進運動のみを表しているものとする。
- T2は、約300 Kである。
- 各曲線における最大確率速度(頂点における速度)は、それぞれの平均の速さより小さい。
- 分子量が2倍、温度T1の理想気体における分布曲線は、曲線Aと比べて、右側にシフトし広がる。
- 温度が高くなれば、速さの分布は広がる。




コメント
コメント一覧 (1件)
[…] 第100回 問92 […]