下図は、ある純物質のエントロピーの温度依存性を示したグラフである。純物質の状態に関する記述のうち、正しいのはどれか。2つ選べ。
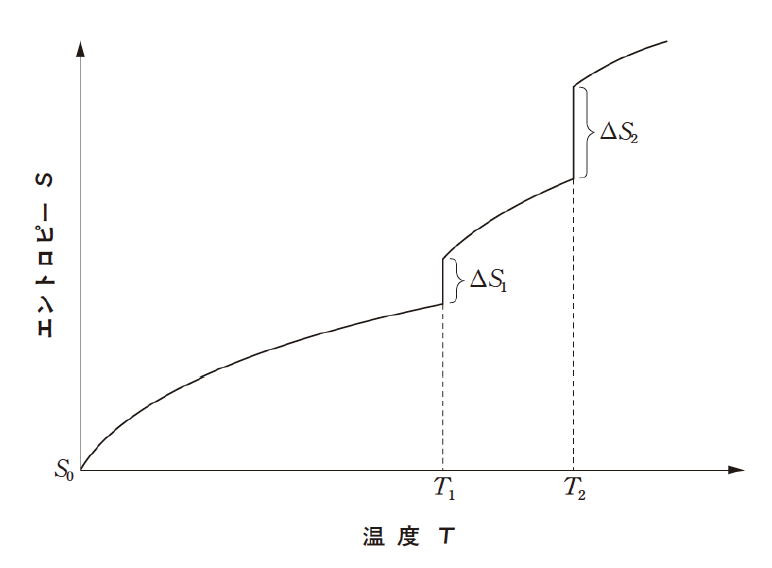
- 物質の温度Tが0<T<T1の領域では、気体の状態にある。
- 物質の温度TがT1<T<T2の領域では、固体の状態にある。
- 温度ゼロにおけるエントロピー(S0)は、物質によっては負になる場合がある。
- ΔS2・T2の大部分は、気化エンタルピーの変化量に由来する。
- 物質によらず、ΔS1・T1<ΔS2・T2の関係が成り立つ。
下図は、ある純物質のエントロピーの温度依存性を示したグラフである。純物質の状態に関する記述のうち、正しいのはどれか。2つ選べ。

解答 解説 2 誤 3 誤 4 正 5 正解答・解説
4、5
1 誤
物質は温度の上昇に伴って、固体→液体→気体へと状態変化する。このことから、0<T<T1の領域では固体の状態、T1<T<T2の領域では液体の状態、T2<Tの領域では気体の状態にある。
解説1参照
温度ゼロにおけるエントロピー(S0)は、物質によらず0である(熱力学第三法則)。
T2は液体から気体に変化する温度(沸点)である。沸点において物質は平衡状態にあるため、ΔG=ΔH-T・ΔS=0が成立する。前記の式を変換すると、ΔH=T・ΔSとなることから、ΔS2・T2の大部分は、気化エンタルピーの変化量(ΔH2)に由来する。
ΔS1・T1は融解エンタルピー、ΔS2・T2は蒸発エンタルピーを示しており、物質によらず融解エンタルピー<蒸発エンタルピーであることから、物質によらず、ΔS1・T1<ΔS2・T2の関係が成り立つ。
コメント
コメント一覧 (1件)
[…] 第101回 問91 […]